Rev. Colomb. Nefrol. 2018;5(1): 36 - 42. http://www.revistanefrologia.org
Investigación original
doi: http://dx.doi.org/10.22265/acnef.5.2.295
José Lucas Daza1,*, Yaroslad De La Cruz1, Cintia Marín1, Martín Zapata1, Fernando Segovia1, Luis José Daza1, Graciela De Rosa2, John Galindo3
1 Servicio de Nefrología del Hospital de Clínicas, Universidad de Buenos Aires, Argentina
2 Servicio de Patología del Hospital de Clínicas, Universidad de Buenos Aires, Argentina
3 Médico cirujano, Universidad Pedagógica y Tecnológica de Colombia, Boyacá, Colombia
Resumen
Introducción: la artritis reumatoidea (AR) es uno de los síndromes clínicos con mayor frecuencia dentro de las afecciones reumatológicas y su asociación con las enfermedades glomerulares es poco frecuente.
Objetivo: describir los hallazgos histopatológicos en las biopsias renales en pacientes con artritis reumatoidea y correlacionarlos con las manifestaciones clínicas y de laboratorio al inicio, a los 6 meses y al año de seguimiento.
Pacientes y métodos: es un estudio observacional retrospectivo realizado en un hospital Universitario en Buenos Aires, Argentina. Se incluyeron 41 pacientes con diagnóstico de artritis reumatoidea de acuerdo a los criterios establecidos por el Colegio Americano de Reumatologia publicados en 1987; en un período de 20 años. Se incluyeron diagnósticos histopatológicos de nefropatía membranosa (NM), enfermedad de cambios mínimos (ECM), amiloidosis secundaria (AA), gloméruloesclerosis focal y segmentaria (GEFS); glomerulopatía mesangial (GPM) y glomerulonefritis con proliferación extracapilar (GNEC). Las características clínicas, de laboratorios, la descripción histopatológica, los años de evolución de la artritis reumatoidea y los diferentes tratamientos fueron analizados durante los primeros 6 meses y al año del seguimiento. Con esto, se buscó determinar la progresión de la insuficiencia renal, calculada a través de la fórmula de MDRD (Modification of Diet in Renal Disease) de 4 variables y el aumento de la proteinuria.
Resultados: el hallazgo histológico más frecuente fue la amiloidosis, con un 34.1 % (n=14), seguido de la glomerulopatía mesangial (21,9 %, n=9), la nefropatía membranosa (19,5 %, n=8), la glomerulonefritis con proliferación extracapilar (12,1 %, n=5), la glomeruloesclerosis focal y segmentaria (7,3 %, n=3) y enfermedad de cambios mínimos (8,2 %, n=2). El síndrome nefrótico fue la forma de presentación más frecuente en los pacientes con amiloidosis (en un 85,7 % de los casos), la microhematuria se presentó en el 100 % de los pacientes con GPM y en el 80 % de los pacientes con GNEC. En el 85,7 % de los pacientes con AA, se presentó fibrosis intersticial moderada a severa, mientras que en la GNEC y la NM la fibrosis se observó en un 80 % y 40 % respectivamente. Se evaluó la proteinuria de 24 horas, la creatinina y la filtración glomerular estimada por MDRD a los 6 y a los 12 meses. Se concluyó que los pacientes con AA, GEFS y GNEC presentaron mayor progresión de la insuficiencia renal a los 12 meses. Lo contrario sucedió en los pacientes con enfermedad de cambios mínimos (ECM) y glo-merulopatía mesangial (GPM), los cuales tenían una menor progresión de la insuficiencia renal al año de seguimiento. Hubo una correlación entre las glomerulopatías que tenían mayor deterioro de la función renal en las cuales se observó a su vez, mayor compromiso tubulointersti-cial, (este fue el caso de la amiloidosis). Las glomerulopatías que presentaban mayor proteinuria al inicio eran la nefropatía membranosa, la amiloidosis y la enfermedad de cambios mínimos. Tanto la nefropatía membranosa como la enfermedad de cambios mínimos, tenía remisión parcial tras un año, a diferencia de la amiloidosis, la cual presentaba progresión de la proteinuria a los 12 meses de seguimiento.
Conclusión: las glomerulopatías que presentaron mayor progresión de la insuficiencia renal al año, con base en la estimación por MDRD4, tenían en la biopsia renal mayor compromiso tubulointersticial. Estas fueron la amiloidosis secundaria, la glomeruloesclerosis focal y segmentaria, y glomerulonefritis con proliferación extracapilar. Por el contrario, las de mejor evolución respecto al grado de proteinuria y tasa de filtrado glomerular determinado por MDRD4, fueron la glomerulopatía mesangial, la enfermedad de cambios mínimos y la nefropatía membranosa.
Palabras clave: artritis reumatoidea, glomerulopatías, sedimento urinario, MDRD, insuficiencia renal.
doi: http://dx.doi.org/10.22265/acnef.5.2.295
Abstract
Introduction: Rheumatoid arthritis is one of the most common clinical syndromes within rheumatological conditions and its association with glomerular diseases is rare.
Objective: To describe the histopathological findings in renal biopsies in patients with rheumatoid arthritis and to correlate them with the clinical and laboratory manifestations at the beginning, at 6 months and at one year of follow-up.
Patients and Methods: This is a retrospective observational study conducted in the Hospital de Clinicas “Jose De San Martin” in Buenos Aires, Argentina; Where we included 41 patients diagnosed with RA (ACR 1987) in a period of 20 years. Histopathological diagnoses of membranous nephropathy (MN), minimal change disease (MCD), secondary amyloidosis (AA), focal and segmental glomerulosclerosis (FSGS); mesangial glomerulopathy (MGP) and glomerulonephritis with extracapillary proliferation (GNEC) were included. Histopathological description, different treatments, years of evolution of rheumatoid arthritis Clinical and laboratory characteristics were analyzed during the first 6 months and one year of follow-up in order to determine the progression of renal failure calculated through the formula of MDRD of 4 variables (Modification of diet in renal disease) and the increase of proteinuria.
Results: The most frequent histological finding was amyloidosis with 34,1 % (n=14), followed by mesangial glomerulopathy 21,9 % (n=9), membranous nephropathy 19,5 % (n=8), glomerulonephritis with extracapillary proliferation 12,1 % (n=5), focal and segmental glomerulosclerosis 7,3 % (n=3) and minimal change disease 8,2 % (n=2). Nephrotic syndrome was the most frequent presentation in patients with amyloidosis in 85,7 %, microhematuria occurred in 100 % of patients with MPG and in 80 % of patients with GNEC. In patients with AA, moderate to severe interstitial fibrosis occurred in 85,7 %, followed by GNEC and NM with 80 % and 40 % respectively. The 24-hour proteinuria, creatinine and glomerular filtration rate estimated by MDRD at 6 months and 12 months were evaluated. Concluding, that patients with AA, FSGS and GNEC had greater progression of renal failure at 12 months; the opposite occurred in patients with minimal change disease (MCD) and mesangial glomerulopathy (MGP) who had a lower progression of renal failure at one year of follow-up; There was a correlation in the glomerulopathies that had greater deterioration of the renal function had greater interstitial tubule involvement as was the case of amyloidosis. The glomerulopathies that presented greater proteinuria at the beginning were membranous nephropathy, amyloidosis and minimal change disease. Both membranous nephropathy and minimal change disease had partial remission at one year, in contrast to amyloidosis, which showed progression of proteinuria at 12 months of follow-up.
Conclusion: The glomerulopathies that presented greater progression of renal failure at 1 year based on the estimation by MDRD 4, had a higher renal tubular interstitial involvement in renal biopsy and these were amyloidosis (AA), segmental focal glomerulosclerosis (FSGS), glomerulonephritis with proliferation extracapillary On the other hand, those with the best evolution in relation to the degree of proteinuria and the glomerular filtration rate determined by the MDRD4 equation were mesangial glomerulopathy, minimal change disease, and membranous nephropathy.
Key words: Rheumatoid arthritis, glomerulopathies, urinary sediment, MDRD, renal failure.
doi: http://dx.doi.org/10.22265/acnef.5.2.295
Referenciar este artículo: Daza JL, De La Cruz Y, Marín C, Zapata M, Segovia F, Daza LJ, De Rosa G, Galindo G. Evolución de las glomerulopatías asociadas a la artritis reumatoidea. Rev. Colomb. Nefrol. 2018;5(1): 36-42. doi: http://dx.doi.org/10.22265/acnef.5.2.295
*Correspondencia: Lucas Daza, drlucasdaza@gmail.com
Recibido: 10-11-17 • Aceptado: 15-01-18 • Publicado en línea: 18-01-18
Las enfermedades reumatológicas como el lupus eritematoso sistémico y la esclerosis sistémica impactan de forma directa a los problemas renales. La artritis reumatoidea (AR) es uno de los síndromes clínicos con mayor frecuencia dentro de las afecciones reumatológicas y su asociación con las enfermedades glomerulares es poco conocida. Las manifestaciones renales en la AR son muy variadas y pueden ser debidas a la misma enfermedad o a los fármacos utilizados para su tratamiento1. La AR ha sido asociada con una amplia variedad de desórdenes renales, debido a su componente inflamatorio crónico, la exposición a drogas o a la toxicidad de las mismas2.
En un estudio realizado por Yoshinaga et al., sobre 154 pacientes con AR ambulatorios, se encontró que las alteraciones urinarias tales como la proteinuria y la microhematuria se presentaban en un tercio de los casos. Adicionalmente, los indicadores de daño tubular fueron altos tanto en histología, como en los niveles urinarios con b2 microglobulina y de N-acetil-beta-D-glucosaminidasa3. La principal glomerulopatía fue la amiloidosis, que tenía mayor compromiso tubular y peor evolución.
La glomerulopatía mesangial y la nefropatía membranosa derivada del tratamiento con sales de oro y penicilamina han sido descritos como los hallazgos histopatológicos más frecuentes en pacientes con AR y disfunción renal. La amiloidosis sistémica es la causa más frecuente de proteinuria nefrótica y falla renal en pacientes con AR4. La prevalencia de hallazgos clínicos como la hematuria ha sido reportada entre un 5 % a 35 %; y la proteinuria, entre 3 % y 7 %.
La disfunción renal es ocasionalmente intratable. Algunos pacientes desarrollan insuficiencia renal crónica y llegan a requerir de terapia de remplazo renal. Este tipo de insuficiencia es uno de los principales factores pronóstico en los pacientes con AR5.
La prevalencia actual de falla renal crónica es difícil de establecer, dados los numerosos factores que interfieren en la función renal de los pacientes con AR. Se han reportado casos de insuficiencia renal como causa de muerte entre el 3 % y el 20 % de los casos6,7. Sin embargo, estos estudios no reflejan la magnitud real de la enfermedad renal en pacientes con AR y no hay estudios clínicos controlados para determinar la incidencia de la enfermedad renal en pacientes con AR.
El objetivo de este estudio fue describir los hallazgos histopatológicos en las biopsias renales de los pacientes con AR y correlacionarlos con las manifestaciones clínicas y de laboratorio (incluyendo la forma de presentación, el sedimento urinario, y el tratamiento con sales de oro y antiinflamatorios no esteroideos —AINES—). Se realizó un seguimiento durante 12 meses para evaluar cuáles glomerulopatías presentaban peor evolución, con base en el filtrado glomerular calculado a través de la fórmula de 4 variables de MDRD.
Se analizaron las biopsias renales de los pacientes con AR de la división de nefrología del Hospital de Clínicas José de San Martín (HCJSM), de la ciudad de Buenos Aires. Estas fueron realizadas entre enero de 1989 y enero del 2010. El diagnóstico de AR se realizó de acuerdo a los criterios del Colegio Americano de Reumatología de 1987.
Se encontraron diferentes enfermedades glomerulares en un total de 41 pacientes. Se incluyeron la glomerulopatía mesangial (GM), la glomerulonefritis con proliferación extracapilar (GNEC), la nefropatía membranosa (NM), la amiloidosis secundaria (AA), la glomeruloesclerosis focal y segmentaria (GEFS), y la enfermedad de cambios mínimos (ECM). Durante la revisión, se analizaron los años de evolución de la AR, los tratamientos recibidos con sales de oro y antiinflamatorios no esteroideos (AINES), la presentación clínica, los hallazgos histopatológicos, la fibrosis intersticial y la atrofia tubular. Esta última se consideró moderada cuando el compromiso era más del 25 %; y severa, cuando era mayor del 50 %.
La proteinuria en 24 horas, la creatinina plasmática y el filtrado glomerular fueron calculados a través de la formula de MDRD de 4 variables. El sedimento urinario fue realizado por nefrólogos entrenados en esta práctica.
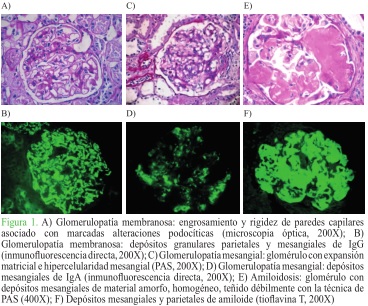
Por otra parte, la hematuria dismórfica se definió como la presencia de 3 o más glóbulos rojos por campo de alto aumento (40x) y más del 40 % de dismorfismo8,9. Se realizó un seguimiento por 12 meses, con el objetivo de observar qué grupo tenía peor evolución, según las mediciones con la fórmula MDRD. (Figura 1).
Criterios de inclusión:
Criterios de exclusión:
Las variables cualitativas se estudiaron a través de frecuencias relativas y absolutas; las variables cuantitativas, con medias aritméticas y desviaciones estándar. Se analizaron las diferentes variables de laboratorio y presentación clínica. Así mismo, se analizó la evolución a los 6 meses y 12 meses de la proteinuria de 24 horas, la creatinina plasmática y el MDRD.
Fueron incluidos los pacientes con diagnóstico de AR según criterios del Colegio Americano de Reumatología, y que tenían biopsia con enfermedad glomerular en el periodo comprendido entre enero de 1989 y enero de 2010. Se hizo un seguimiento completo de las historias clínicas hasta los 12 meses. El sedimento de orina fue analizado por nefrólogos del servicio del HCJSM. Se excluyeron aquellos pacientes que mostraban una coexistencia de otras enfermedades reumatológicas y biopsias renales sin inmunofluorescencia.
La población objeto de estudio era de género femenino en un 68 % (n=28) y masculino en un 32 % (n=13). El hallazgo histológico más frecuente fue la amiloidosis (34,1 %, n=14), seguido de la glomerulopatía mesangial (21,9 %, n=9), la nefropatía membranosa (19,5 %, n=8), la glomerulonefritis con proliferación extracapilar (12,1 %, n=5), la gloméruloesclerosis focal y segmentaria (7,3 %, n=3), y la enfermedad de cambios mínimos (4,87 %, n=2). Las glomerulopatías que presentaban mayor proteinuria al inicio eran la nefropatía membranosa, la amiloidosis y la enfermedad de cambios mínimos. Tanto la nefropatía membranosa como la enfermedad de cambios mínimos, tenían remisión parcial al año, a diferencia de la amiloidosis, que evidenció progresión de la proteinuria a los 12 meses de seguimiento.
Con respecto a las formas de presentación clínica y los hallazgos urinarios, el 48,7 % (n=20) se presentó como síndrome nefrótico. La ECM y la AA fueron las glomerulopatías con mayor frecuencia. Por el contrario, la presentación de microhematuria fue más frecuente en la GPM, en un 100 % de los casos (n=9); y en la GNEC, en un 80 % (n=4).
En lo referente al tiempo de evolución, el número de años fue mayor para los pacientes con AA, con aproximadamente 15 años (14,5±7,8). De manera similar, ocurrió para la ECM y la GNEC, con aproximadamente 7,5 años (7,5±6,3 y 7,4±7,9; respectivamente) (Tabla 1).
Las glomerulopatías que presentaron mayor progresión de la insuficiencia renal al año de seguimiento (con base en la estimación por MDRD); y que tenían en la biopsia renal mayor compromiso tubulointersticial, fueron la amiloidosis, la glomerulonefritis con proliferación extracapilar, y la glomeruloesclerosis focal y segmentaria (Tabla 2).
Existen unos pocos estudios que describen el deterioro de la función renal en pacientes con AR. Un estudio de cohorte transversal de 604 pacientes finlandeses con AR documentó nefropatía (definida como microhematuria, proteinuria o insuficiencia renal) en el 17 % de los casos. De los 604 pacientes, 54 tenían hematuria aislada, 27 tenían proteinuria aislada y 7 tenían microhematuria y proteinuria. La insuficiencia renal crónica definida por los niveles de creatinina séricos se encontró en un total de 29 pacientes, de los cuales 15 no tenían hematuria ni proteinuria1.
En nuestro estudio, se analizó la proteinuria medida en 24 horas, la creatinina plasmática y la filtración glomerular estimada por MDRD4 al momento de la biopsia, a los 6 y 12 meses. Se evidenció que los pacientes que tenían amiloidosis presentaban mayor grado de incremento en la proteinuria e insuficiencia renal a los 6 y 12 meses. Así mismo, se observó que hubo un descenso del filtrado glomerular, evolutivamente, a los 6 y a los 12 meses para la GEFS. Sin embargo, por lo pequeño de la muestra, no se pudieron hacer comparaciones estadísticas.
Las limitaciones de nuestro estudio son claras, pues se tuvo un reducido tamaño de muestra, hubo un enfoque retrospectivo y un seguimiento de tan solo 12 meses. Sin embargo, se obtuvieron datos de una población local.
Las enfermedades renales reportadas en la literatura y más comúnmente observadas en pacientes con artritis reumatoidea que se sometieron a biopsia renal, son la glomerulopatía mesangial, la amiloidosis y la nefropatía membranosa, cuya correlación se mantiene en nuestro estudio.
El sedimento urinario es una herramienta útil, porque la presencia de microhematuria glomerular es más prevalente en unas entidades que otras (mayor en la glomerulopatía mesangial y la glomerulonefritis con proliferación extracapilar, en nuestra cohorte). Las glomerulopatías que presentaron mayor progresión de la insuficiencia renal al año, con base en la estimación por MDRD4, tenían en la biopsia renal mayor compromiso tubulointersticial. Estas eran la amiloidosis, la glomeruloesclerosis focal segmentaria y la glomerulonefritis con proliferación extracapilar. Las de mejor evolución fueron la glomerulopatía mesangial, la enfermedad de cambios mínimos y la nefropatía membranosa.
Los autores declaran que no existe ningún conflicto de interés.
Por medio de este escrito manifestamos no haber recibido financiación de ningún tipo durante el desarrollo y finalización del artículo.
Protección de personas y animales
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos
Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado
Los autores declaran que en este artículo no aparecen datos de pacientes
Anteproyecto, proyecto, recolección y análisis de datos: Yaroslad De La Cruz, Cintia Marín, Martín Zapata, Luis José Daza, John Galindo.
Tutor temático y metodológico: Fernando Segovia. Tutor metodológico y estadística: Dr José Lucas Daza.
Tutor en patología: Graciela De Rosa.
1. Karstila K, Korpela M, Sihvonen S, Mustonen J. Prognosis of Clinical Renal Disease and Incidence of New Renal Findings in Patients with Rheumatoid Arthritis: Follow-Up of a Population-Based Study. Clin Rheumato. 2007;26(12):2089-2095. http://doi.org/10.1007/s10067-007-0625-y
2. Hickson LJ, Crowson CS, Gabriel SE, McCarthy JT, Matteson EL. Development of Reduced Kidney Function in Rheumatoid Arthritis. Am J Kidney Dis. 2014;63(2):206-213. http://doi.org/10.1053/j.ajkd.2013.08.010
3. Yoshinaga Y, Nishiya K, Yamamura M, Hatano M, Ogura T, Takaoka M, et al. Study of Urinary findings and Renal Functions in Patients with Rheumatoid Arthritis [en Japonés]. Kidney Dialysis. 1989;26:477-482.
4. Hill AJ, Thomson RJ, Hunter JA, Traynor JP. The Prevalence of Chronic Kidney Disease in Rheumatology Outpatients. Scott Med J. 2009;54(2):9-12. doi: http://doi.Org/10.1258/rsmsmj.54.2.9
5. Symmons DP, Jones MA, Scott DL, Prior P. Long Term Mortality Outcome in Patients with Rheumatoid Arthritis: Early Presenters Continue to Do Well. J Rheumatol. 1998;25(6):1072-1077.
6. Laasko M, Mutru O, Isomaki H, Koota K. Mortality from Amyloidosis and Renal Disease in Patients with Rheumatoid Arthritis. Ann Rheum Dis. 1986;45(8):663-667.
7. Adu D, Tse WY. Rheumatoid Arthritis, Mixed Connective Tissue Disease, and Polymyositis. in: Adu D, Emery P, Madaio MP, editores. Rheumatology and the Kidney. New York: Oxford University Press; 2001. p. 293-302.
8. Fogazzi G. The Urinary Sediment. An Integraded View. 3a ed. Milan: Elsevier; 2009.
9. Fogazzi GB, Grignani S: Urine microscopic analysis: An art abandoned by nephrologists? Nephrol Dial Transplant. 1998;13:2485-2487.
10. Hall CL, Fothergill NJ, Blackwell MM, Harrison PR, MacKenzie JC, MacIver AG. The Natural Course of Gold Nephropathy: Long Term Study of 21 Patients. Br Med J (Clin Res Ed). 1987;295(6601):745-748.
11. Hall CL, Jawad S, Harrison PR, MacKenzie JC, Bacon PA, Klouda PT, MacIver AG. Natural Course of Penicillamine Nephropathy: A Long Term Study of 33 Patients. Br Med J (Clin Res Ed). 1988;296(6629):1083-1086.
12. Bourke BE, Woodrow DF, Scott JT. Proteinuria in Rheumatoid Arthritis-Drug-Induced or Amyloid? Ann Rheum Dis. 1981;40(3):240-244.
13. Helin HJ, Korpela MM, Mustonen JT, Pasternack AI. Renal Biopsy Findings and Clinicopathologic Correlations in Rheumatoid Arthritis. Arthritis Rheum. 1995;38(2): 242-247.